tDCS等无创脑刺激技术(NIBS)与肠道菌群作用机制研究
文章图片
文章图片
文章图片
【背景分析】
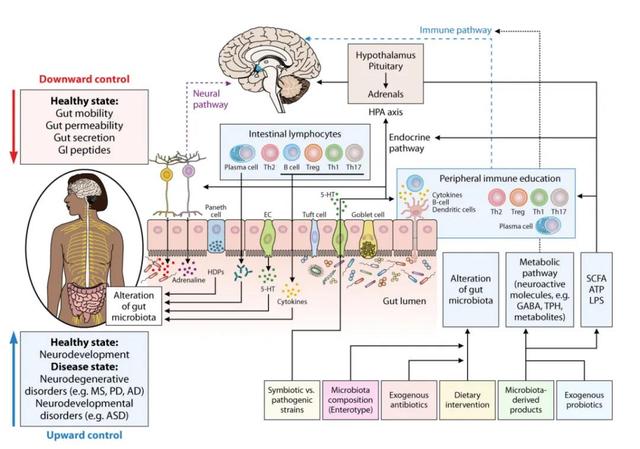
【tDCS等无创脑刺激技术(NIBS)与肠道菌群作用机制研究】根据近两年国内外的研究 , 发现肠道菌群失衡 , 与神经系统疾病的发生和发展有关 , 即“微生物-肠-脑轴”Microbiota-gut-brain axis(MGBA) , 或“肠-脑轴”Gut–brain axis(GBA) 。 例如儿童及青少年期常见的如多动症(ADHD)、抽动症(TS)、自闭症(ASD)等 , 老年期常见的如阿尔茨海默病、帕金森病等 。
如上图所示 , 对比了健康人肠道菌群 , 和神经系统疾病患者肠道菌群的明显差异 。 如相比健康人群 , 神经系统疾病患者肠道中双歧杆菌、抗炎细菌(粪球菌属、玫瑰球菌属、蓝氏菌属等)水平较低 。
【无创脑刺激技术】
无创脑刺激技术也叫非侵入性脑刺激(noninvasive brainstimulationNIBS)就是利用电流、磁场等非侵入性技术 , 调节大脑相关功能区的兴奋性 , 改善神经连接 , 达到治疗目的的技术 。
常见的如经颅直流电刺激(transcranial directcurrentstimulatiointDCS) , 经颅磁刺激(transcranial magnetic stimulation TMS)等 。
【无创脑刺激技术(NIBS)对肠道菌群的影响】
人类胃肠道微生物群包含超过100多种细菌 , 包括两种主要的细菌门 , 即厚壁菌门和拟杆菌门 , 以及较少的放线菌门、梭杆菌门、变形菌门和疣微菌门 。
根据2020年发表在《Brain Stimulation》一篇报道 , 患者通过为期10周 , 每周2次(治疗方案为2mA , 20分钟) , 治疗后发现患者拟杆菌(bacteroidetes)/厚壁菌(fifirmicutes)的比率从8.5下降到了5.2 , 下降比例为38.8%;同时 , 罗斯拜瑞氏菌(Roseburia?intestinalis)、普拉梭菌(Faecalibacterium Prausnitzii)、拟杆菌(bacteroidetes)水平明显升高 , 并持续超过10周 。
肠道菌群和大脑之间 , 通过肠-脑轴(GBA)建立联系
研究表明 , 肠道菌群通过刺迷走神经(VN)和肠神经系统(ENS)的神经元 , 在大脑和胃肠道菌群之间建立直接的神经连接 。 另外 , 迷走神经的激活水平 , 反应了身体的抗炎水平 , 炎症水平升高 , 会损害肠道上皮屏障的完整性和通透性 , 导致有害物质进入血液 , 损害神经系统 。
研究人员认为 , tDCS干预通过影响迷走神经 , 提高了抗炎症水平 , 进而恢复肠道上皮屏障的完整性和通透性、改善了肠道菌群结构 , 改善肠道生态环境 。 而肠道生态系统改善 , 促进了神经递质合成(如去甲肾上腺素、多巴胺、γ-氨基丁酸等) , 再通过“肠-脑轴”(GBA)机制 , 影响大脑相关区域(如前额叶等)的激活/抑制水平 , 改善症状 。
【最新研究进展】
2021年 , 米兰大学医学院、欧洲肿瘤研究所的研究人员 , 在《Molecular Sciences》上发表的研究报告 , 总结了无创脑刺激技术(NIBS)和肠道菌群关系的最新研究成果 。
研究团队将参与试验的22名患者 , 分为HF组、LF组和伪刺激组 。 HF组、LF组分别采用2种无创脑刺激技术(NIBS)进行干预 , 伪刺激组每次干预30秒后即停止 。 在进行每周3次、连续5周 , 总计15次治疗后 , 检查3组患者肠道菌群、神经递质(肾上腺素、去甲肾上腺素、GABA、血清素等)变化 。
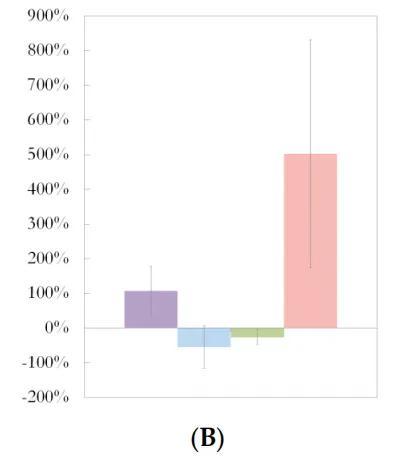
下面三张图中 , 紫色代表普拉梭菌(Faecalibacterium)、蓝色代表另枝杆菌(Alistipes , 是拟杆菌的一种)、浅绿色代表乳酸杆菌(Lactobacillus)、粉色代表梭状杆菌(Clostridium) 。
如上图所示 , HF组主要菌群变化情况 , 可以看出普拉梭菌、另枝杆菌明显增加 , 乳酸杆菌明显降低 , 梭状杆菌也呈现增加的趋势;
如上图所示 , LF组主要菌群变化情况 , 普拉梭菌略有增加 , 另枝杆菌、乳酸杆菌略有降低 , 而梭状杆菌增加最为明显;
如上图所示 , 伪刺激组中 , 乳酸杆菌出现了明显增长 。
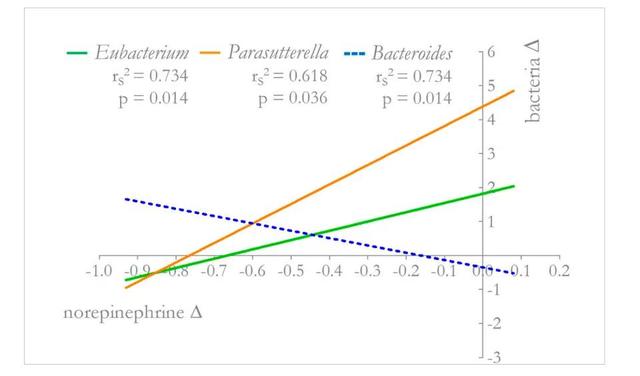
如上图所示 , 分析了去甲肾上腺水平和拟杆菌属(Bacteroides)、真杆菌属(Eubacterium)、副萨特氏菌属(Parasutterella)丰度变化的相关性 。
推荐阅读
- 涨涨涨!杭州多地爆满,预约已排到下周!网友激动:等了3年啦
- 王思聪打人登上热搜?法律面前人人平等,“钞能力”也不例外
- 南阳|南阳五朵山等7家景区联合发出邀请 辞旧迎新原无论天南海北 回家过年何须辨襄阳南阳
- 泡椒加盟费城!76人与快船等四队商讨交易!
- 王思聪等4人在上海打人致轻微伤被暂缓拘留,最终结果将会如何
- 陈继志等人连人带“伞”一起拔除
- 核酸亭,等待“再就业”
- 股市:郑州煤电、天威视讯、广博股份等六家公司重要公告(1.12)
- 古镇|天青色等烟雨, 而“江南”,在等你。
- 惨败太阳,勇管表情严肃,三方交易迫在眉睫,马刺爵士已等候多时